分享:α-FeOOH 和α-Fe2O3 纳米棒的制备及其对高氯酸铵热分解的催化作用
陈丽娟1,黄 惠2
(1.福建船政交通职业学院安全与环境学院,福州350007;2.福州大学机械工程及自动化学院,福州350002)
摘 要:以FeSO4·7H2O和CH3COONa·3H2O为原料,采用水热方法制备α-FeOOH 纳米棒, 将所得α-FeOOH 纳米棒于250℃烧结2h制备α-Fe2O3 纳米棒,采用差热-热重分析法研究了制 备的α-FeOOH 和α-Fe2O3 纳米棒对高氯酸铵热分解的催化性能。结果表明:在100℃水热反应 6h可制备得到平均直径为18nm的纯相α-FeOOH 纳米棒,再于250℃烧结2h后获得平均直径 为16nm的纯六方相α-Fe2O3 纳米棒;α-Fe2O3 和α-FeOOH 纳米棒对高氯酸铵热分解的催化效 果显著,添加质量分数2%的α-Fe2O3 纳米棒和α-FeOOH 纳米棒可使高氯酸铵的结束分解温度分 别降低40,54℃,高温分解峰值温度分别降低51.1,61.6℃;当α-Fe2O3 纳米棒添加质量分数达到 10%时,高氯酸铵的高温分解峰值温度降低约90.9℃。
关键词:α-Fe2O3 纳米棒;α-FeOOH 纳米棒;高氯酸铵;热分解 中图分类号:O642 文献标志码:A 文章编号:1000-3738(2023)04-0028-05
0 引 言
高氯酸铵是复合固体推进剂的最主要氧化剂, 主要应用于火箭发射的推进剂;其热分解温度越低, 点火延迟时间越短,固体推进剂的燃烧速率就越 高[1-3]。添加纳米催化剂,如纳米 MnO [1]、CuxO [2] 28 陈丽娟,等:α-FeOOH和α-Fe2O3 纳米棒的制备及其对高氯酸铵热分解的催化作用 和Gd2O3 [3]等可以降低高氯酸铵的热分解温度。 纳米材料的催化性能与其形貌、相结构以及比表面 积等密切相关[4-8],特殊形貌如棒状、线状等纳米材 料相比于纳米颗粒表现出更好的催化性能。典型的 纳米棒状材料有ZnO 纳米棒[5]、SnO2 纳米棒[8]和 α-Fe2O3 纳米棒[9]等。α-FeOOH 和α-Fe2O3 金属 氧化物由于无毒、性质稳定,广泛用作各种催化 剂[10-15]。然而,α-FeOOH 和α-Fe2O3 纳米棒的制 备方法 相 对 复 杂,一 般 都 需 要 有 机 溶 剂 或 者 模 板[9,15-17],因此用简便的水热方法制备α-FeOOH 和 α-Fe2O3 纳米棒并研究其性能显得尤为重要。 作者 根 据 文 献 [18],以 FeSO4·7H2O 和 CH3COONa·3H2O 为原料,摸索水热法制备 αFeOOH 纳米棒的条件,并将α-FeOOH 纳米棒在 250℃进行烧结获得α-Fe2O3 纳米棒,通过差热-热 重方法探讨了α-FeOOH 和α-Fe2O3 纳米棒对高氯 酸铵热分解的催化作用。


1 试样制备与试验方法
试验原料包括 FeSO4·7H2O、CH3COONa· 3H2O和高氯酸铵(AP),均为分析纯,由上海国药 集团化学试剂有限公司提供。将0.02molFeSO4· 7H2O和0.04molCH3COONa·3H2O分别溶解于 75mL去离子水中得到FeSO4 溶液和CH3COONa 溶液;将 FeSO4 溶液逐滴滴加于 CH3COONa溶液 中,充分搅拌0.5h。前期研究发现,该混合溶液在90 ℃下反应较长时间以及100℃下反应5h均没有形 成沉淀物,但在100℃反应6h就形成了结晶产物。 故以100℃作为反应温度。将上述混合溶液转移至 聚四氟乙烯反应釜中,在100 ℃分别反应6h和 24h,自然冷却至室温后离心分离,得到黑色沉淀 物。用蒸馏水充分洗涤黑色沉淀物,在80 ℃烘干 8h,即得到反应产物。将上述反应产物于250℃烧 结2h,得到另一产物。 采用D8Advance型X射线衍射仪(XRD)对干 燥反应产物和烧结产物进行物相分析,采用铜靶, Kα 射线(波长0.15418nm),扫描速率为5(°)· min-1,扫描范围在5°~90°,步长为0.02°。采用 TecnaiG2F20型透射电镜(TEM)观察干燥反应产 物和烧结产物的微观形貌,加速电压为200kV。按 照 AP和产物质量比为98∶2(即产物质量分数为 2%)、总质量为1.5mg取样,置于敞口氧化铝坩锅 中,采用STA449C-QMS403C型热分析与质谱联用 仪进行差热-热重(DTA-TG)分析,加热速率为20℃· min-1,氮气气氛,温度范围在30~500℃。此外,还 改变α-Fe2O3 添加量(质量分数分别为5%,7%, 10%),与AP混合后进行 了DTA-TG分析。

2 试验结果与讨论
2.1 物相组成和微观形貌
由图1可以看出:FeSO4 和 CH3COONa混合 溶液 在 100 ℃ 反 应 6h 后 的 产 物 为 α-FeOOH (JCPDSfile,No.81-0462),没有观察到其他晶相的 存在;在 100 ℃ 反应 24h 后的产物中除了存在 α-FeOOH 外,还 存 在 其 他 杂 相 (菱 形 标 记)。将 100℃反 应 6h 制 备 的 纯 相 产 物 α-FeOOH 于 250℃烧结2h后,所得产物的XRD谱与六方相αFe2O3 相符(JCPDSfile,No.33-0664),没有出现前 驱体α-FeOOH 或者其他晶相Fe2O3 的衍射峰,说 明烧结得到的产物为纯六方相α-Fe2O3。 图1 100℃反应6,24h产物以及100℃反应6h并烧结后产物的XRD谱 Fig 1 XRDpatternsofproductsobtainedbyreactionat100℃for6h a and24h b andby reactionat100℃for6handsintering c 由图2可以看出,100℃反应6h制备α-FeOOH 及其在250℃烧结2h所得的α-Fe2O3 均为纳米棒形 貌,可见α-FeOOH纳米棒经过烧结后仍可保持其原 形貌。各测量30根纳米棒的直径,得到α-FeOOH和 29 陈丽娟,等:α-FeOOH和α-Fe2O3 纳米棒的制备及其对高氯酸铵热分解的催化作用 图3 纯AP及其与质量分数2%α-Fe2O3 和α-FeOOH纳米棒组成混合物的TG和DTA曲线 Fig 3 TG a andDTA b curvesforpureAPandmixturesofAPand2mass%α-Fe2O3andα-FeOOHnanorods 图2 100℃反应6h制备α-FeOOH及其在250℃烧结2h所得 α-Fe2O3 的TEM形貌 Fig 2 TEMmorphologyofα-FeOOHpreparedbyreactionat100℃ for6h a andα-Fe2O3obtainedbysinteringofα-FeOOHat 250℃for2h b α-Fe2O3 的平均直径分别为18nm和16nm,可见烧 结前后产物的直径相差不大。综上可知:将物质的量 比为1∶2的FeSO4·7H2O和CH3COONa·3H2O混合 后在100℃反应6h,可制备得到纯相α-FeOOH纳米 棒;将制备的纯相α-FeOOH纳米棒在250℃烧结2h 后,可制备得到纯六方相α-Fe2O3 纳米棒。
2.2 对AP热分解的催化作用
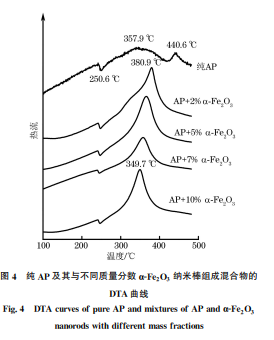
由图3(a)可以看出,纯AP的开始分解温度 和结束分解温度分别为363,434℃,添加α-FeOOH 和α-Fe2O3 纳米棒后其开始分解温度和结束分解温 度均降低。其中,添加α-Fe2O3 纳米棒后的开始和 结束分解温度分别降低 33 ℃ 和 40 ℃,添加 αFeOOH 纳米棒后分别降低了33℃和54℃。添加 α-FeOOH 纳 米 棒 后 的 开 始 分 解 温 度 与 添 加 αFe2O3 纳米棒相同,但结束分解温度下降幅度更大, 说明α-FeOOH 纳米棒的催化效果更好。 纯 AP在升温过程中会出现1个相转变吸热峰 (正交相向立方相转变)和2个分解放热峰(低温分 解和高温分解)[1]。由图3(b)可以看出:纯 AP的 相转变温度约为250.6℃,357.9℃处为其低温分解 放热峰,440.6 ℃处为其高温分解放热峰;添加αFeOOH 和α-Fe2O3 纳米棒对 AP的相转变温度几 乎没有影响,仍保持在250.6℃,与添加许多其他纳 米催化剂的结果一样[1-3,19-22];但是,添加α-FeOOH 和α-Fe2O3 纳米棒后AP热分解的低温放热峰消失, 只出现一个对应于高温分解的放热峰,与添加纳米 CoC2O4 [21]和 MnFe2O4 等现象一致[22],并且高温分 解峰值温度显著降低,分别降低61.6℃和51.1℃。 纳米材料的催化性能与其添加量密切相关[23]。 由图4可以看出:随着α-Fe2O3 纳米棒含量的增加, AP的高温分解峰值温度逐渐降低,当α-Fe2O3 纳 米棒添加量(质量分数)达到10%时,高温分解峰值 温度降低约90.9℃。 综上可知,添加α-Fe2O3 和α-FeOOH 纳米棒 后,AP的高温分解温度显著降低。根据 AP热分解 的电子理论[1,3,21],添加α-Fe2O3 和α-FeOOH 纳米 棒引入的活性金属Fe3+ 可作为电子转移的桥梁,促 进电子从ClO4 向NH+ 4 转移,加快AP的固相反应 速率,从而降低高温分解温度。另外,由于α-Fe2O3 和α-FeOOH 纳米棒的比表面积大,可以提供更多 的活性点位,使得 AP的电子转移速率提高,从而加 30 陈丽娟,等:α-FeOOH和α-Fe2O3 纳米棒的制备及其对高氯酸铵热分解的催化作用 图4 纯AP及其与不同质量分数α-Fe2O3 纳米棒组成混合物的 DTA曲线 Fig.4 DTAcurvesofpureAPandmixturesofAPandα-Fe2O3 nanorodswithdifferentmassfractions 快 AP的热分解。
3 结 论
(1)将物质的量比为1∶2的 FeSO4·7H2O 和 CH3COONa·3H2O混合并在100℃下反应6h后, 成功制备得到平均直径为18nm 的纯相α-FeOOH 纳米棒,将其于250℃烧结2h获得直径为16nm 的纯六方相α-Fe2O3 纳米棒。 (2)α-FeOOH 和α-Fe2O3 纳米棒的添加对高 氯酸铵的相转变温度没有影响,但是降低了其开始 和结束分解温度,添加α-Fe2O3 纳米棒后的开始和 结束分解温度分别降低 33 ℃ 和 40 ℃,添加 αFeOOH 纳米棒后分别降低了33 ℃和54 ℃。此 外,添加α-FeOOH 和α-Fe2O3 纳米棒后高氯酸铵 的低温分解放热峰消失,高温分解放热峰向低温方 向移动,对应的峰值温度分别低61.6℃和51.1℃, 可见α-FeOOH 纳米棒对高氯酸铵热分解的催化效 果更好。 (3)α-Fe2O3 纳米棒对高氯酸铵热分解的催化 作用随着其添加量的增加而提高,当添加量(质量分 数)达到10%时,高氯酸铵的高温分解峰值温度可 降低约90.9℃。
来源:材料与测试网







